


21日,三生制药发布的2019年上半年业绩表现:公司在2019年上半年继承保持强劲增添,研发投入一连加大。今朝,公司在研生物肿瘤药物包围HER2, CD20, PD1, VEGF和EGFR等重要靶点,自身免疫和炎症疾病治疗生物药物包围抗TNFa,IL17A,IL5, IL4R, 和 IL1b抗体等,同时公司研发还聚焦新型的下一代生物疗法,包罗措施化细胞疗法,免疫搜查点克制剂,巨噬细胞搜查点调理剂,双特异性抗体以及定位于公司综合抗体产物线的连系疗法。
财报数据表现:2019年上半年,公司共实现业务收入人民币约26.43亿元,比客岁同期增添21.6%;毛利约人民币21.85亿元,比客岁同期增添25.1%;正常化EBITDA人民币约10.18亿元,比客岁同期增添21.4%;正常化净利润人民币约7.52亿元,比客岁同期增添34.1%;研发投入约2.6亿元,比客岁同期增添48.2%。
制止2019年上半年,公司有32项在研产物,个中22种国度一类新药,涵盖肿瘤科11项、自身免疫性疾病12项、肾科6项、代谢2项、皮肤科1项。同时,公司继承稳步拓展对外相助。2019年,韩国Samsung Bioepis、美国Verseau、台湾TLC相继与公司告竣计谋相助,配合寻求更多打破性疗法,进一步富厚现有产物及在研产物组合。
2019年上半年,公司4种焦点产物特比澳、益赛普、益比奥和赛博尔在各自的治疗规模保持市场领先职位。按照IQVIA数据,用于治疗血小板镌汰症的特比澳作为当今环球独一贸易化的重组人血小板天生素产物,在2019上半年贩卖额增进42%,市场份额增至72.5%;用于治疗类风湿性枢纽炎、强直性脊柱炎及银屑病的益赛普贩卖额增进13.2%,市场份额为61.9 %;这两种产物仍处于产物生命周期的早期阶段,在中国的渗出率较低,临床需求远未获得满意,将来市场潜力庞大;而公司两种重组人促红素产物益比奥和赛博尔贩卖额增进5.8%,市场份额增为41.3%。
2019年6月25日,我国第一个获批单抗重组人源化抗CD25单克隆抗体打针液健尼哌得到国度药监局揭晓的中国药品GMP证书,今朝公司正起劲筹备该产物的上市贩卖。该产物用于提防肾移植引起的急性排异回响,可明显进步移植器官的存活率,改进患者保留质量。
按照最近宣布的2019年新版医保目次,公司多款产物被纳入个中,包罗治疗多种皮肤病的产物丙酸氟替卡松乳膏(适诺),益赛普新增用于成人重度斑块状银屑病顺应症,益比奥新增用于非骨髓恶性肿瘤化疗引起的血虚顺应症,精卵白锌重组人胰岛素(优泌林)由医保乙类升至甲类。公司还将起劲推进其他相干产物进入会谈目次的历程。
研发方面,公司在2019上半年取得了重大盼望,完成了预充式益赛普水针剂(301S)的三期试验,并已向国度药监局递交出产批件且得到受理。
在研生物肿瘤药物产物——HER2, PD1, EGFR等抗体均稳步推进:客岁向国度药监局从头提交新药上市容许申请的治疗乳腺癌的抗HER2单克隆抗体药物302H,今朝已由国度药监局审评中心完成技能检察及临床试验数据现场核查;用于治疗多类癌症的抗PD1抗体609A的临床试验已于本年1月得到美国食药监局的新药临床批件并于4月开始患者入组,本年6月中国国度药监局已受理该产物新药临床批件;治疗肿瘤的抗表皮发展因子受体抗体602完成一期临床试验,并打算开展结直肠癌患者中的后期临床试验。
另一方面,公司自身免疫、炎症及其他疾病治疗生物药物包罗抗TNFa、IL-17A抗体、等也取得了明显盼望:用于类风湿枢纽炎(RA)患者的人源化抗肿瘤坏死因子α抗体产物(SSS07)已完成康健志愿者及RA患者的一期临床试验,今朝正在筹办RA患者及其他炎症性疾病的二期试验;用于中重度斑块状银屑病的抗IL-17A抗体(608)的临床试验于本年7月31日得到国度药监局新药临床批件,即将开展患者入组。
治疗血虚的第二代重组人促红素产物NuPIAO (SSS06)已完成多次一期临床试验,并已开设二期临床试验的患者入组。用于治疗血虚的聚乙二醇长效促红细胞天生素RD001已完成一期临床试验,现正筹办血虚患者的二期试验。特比澳已开始儿科ITP顺应症临床试验,正在举办患者入组,有血小板镌汰风险的肝成果障碍患者在外科围手术期带动的第一期临床试验已完成,即将启动第二期临床试验。
2019上半年,公司继承加速外部相助步骤:与韩国Samsung Bioepis相助开拓SB8贝伐珠单抗在内的多款生物相同药产物;与Verseau相助开拓用于抗多种肿瘤的巨噬细胞免疫调理剂产物;与TLC相助开拓肿瘤、传染等疾病规模的创新微脂体产物。
 乳腺癌容易盯上哪些人?
乳腺癌容易盯上哪些人?  白带发黄是宫颈癌的警示吗?
白带发黄是宫颈癌的警示吗?  超高龄生育,这几件事你准备好了吗?
超高龄生育,这几件事你准备好了吗?  孩子发烧、恶心、呕吐!竟然是心理出了问题
孩子发烧、恶心、呕吐!竟然是心理出了问题  数据显示我国女性平均预期寿命突破80岁
数据显示我国女性平均预期寿命突破80岁  健康早知道:你的子宫还“年轻”吗?
健康早知道:你的子宫还“年轻”吗?  打了胰岛素,血糖为什么没有降?
打了胰岛素,血糖为什么没有降?  多囊卵巢,如何才能尽快怀孕?
多囊卵巢,如何才能尽快怀孕?  女性更年期如何保持健康与美丽?
女性更年期如何保持健康与美丽?  坚持早睡身体会有什么变化?
坚持早睡身体会有什么变化?  抑郁的人,这4类食物尽量少碰,或助改善情绪
抑郁的人,这4类食物尽量少碰,或助改善情绪  多吃3样粗粮,健脾胃,营养滋补暖身
多吃3样粗粮,健脾胃,营养滋补暖身 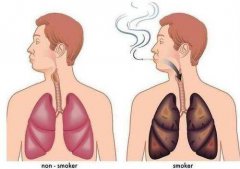 南京一男子每天1包烟4年2次心梗
南京一男子每天1包烟4年2次心梗  小小“杨桃”是个宝,养颜美容抗疲劳
小小“杨桃”是个宝,养颜美容抗疲劳  多吃三种美食,润肠排毒,美容养颜,滋养子宫
多吃三种美食,润肠排毒,美容养颜,滋养子宫  天天吃二甲双胍,为何血糖不降反升?
天天吃二甲双胍,为何血糖不降反升?