

近日,山西振东制药股份有限公司用于治疗多发性硬化症的创新药ZD03获得美国FDA批准开展临床试验, ZD03作为我国具有完全自主知识产权的全新化学结构类型(NCEs)的小分子创新药,获准正式在美开展I期临床试验研究,标志着它在中美同步申报的过程中,迈出了坚实而可喜的一步,开启了创新药研发的新篇章。
ZD03作为我国自主开发的1类创新药,它是一种来源于中药旋覆花的全新药,其先导化合物线叶旋覆花内酯A于2010年由海军军医大学张卫东教授领衔的课题组首先发现,并报道了其抗炎活性。课题组多年来一直致力于抗炎活性中草药的研究,发现旋覆花属多种植物具有显著抗炎活性。通过对12种国产旋覆花属植物进行系统成分研究,鉴定了700余种化合物的分子结构,其中150个为新化合物,包括9种碳骨架类型的倍半萜、7种不同连接片断或连接方式的倍半萜二聚体等。在张教授带领下,课题组从药材到提取物、各极性部位和单体成分的每个中间过程都采用药效学跟踪评价,抗炎活性显著,且在植物中含量丰富的线叶旋覆花内酯A终被发现。
研究表明,线叶旋覆花内酯A在多个炎症模型上有显著的抗炎作用,尤其是对实验性自身免疫性脑脊髓炎(Experimental autoimmune encephalomyelitis,EAE)动物模型有很好的治疗作用,该模型是多发性硬化(multiple sclerosis,MS)的理想动物模型,研究结果已申请专利并获得美国专利授权。随着研究的深入,张教授课题组于2016年报道了线叶旋覆花内酯A的作用靶标为Keap1-Nrf2-ARE抗氧化通路。
研究团队对先导化合物线叶旋覆花内酯A继续进行了成药性评估,为改善其药代动力学特征,制备了其衍生物的盐型ZD03。ZD03具有良好的溶解度,生物利用度相比线叶旋覆花内酯A大幅提高,代谢稳定性好,最终成为候选药物进入临床前研究,经过系统的药学、药效学、药代动力学和安全性评价,于2019年7月5日向FDA递交IND申请,顺利获批临床。
 乳腺癌容易盯上哪些人?
乳腺癌容易盯上哪些人?  白带发黄是宫颈癌的警示吗?
白带发黄是宫颈癌的警示吗?  超高龄生育,这几件事你准备好了吗?
超高龄生育,这几件事你准备好了吗?  孩子发烧、恶心、呕吐!竟然是心理出了问题
孩子发烧、恶心、呕吐!竟然是心理出了问题  数据显示我国女性平均预期寿命突破80岁
数据显示我国女性平均预期寿命突破80岁  健康早知道:你的子宫还“年轻”吗?
健康早知道:你的子宫还“年轻”吗?  打了胰岛素,血糖为什么没有降?
打了胰岛素,血糖为什么没有降?  多囊卵巢,如何才能尽快怀孕?
多囊卵巢,如何才能尽快怀孕?  女性更年期如何保持健康与美丽?
女性更年期如何保持健康与美丽?  坚持早睡身体会有什么变化?
坚持早睡身体会有什么变化?  抑郁的人,这4类食物尽量少碰,或助改善情绪
抑郁的人,这4类食物尽量少碰,或助改善情绪  多吃3样粗粮,健脾胃,营养滋补暖身
多吃3样粗粮,健脾胃,营养滋补暖身 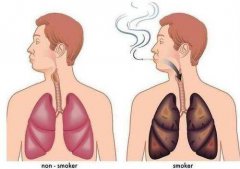 南京一男子每天1包烟4年2次心梗
南京一男子每天1包烟4年2次心梗  小小“杨桃”是个宝,养颜美容抗疲劳
小小“杨桃”是个宝,养颜美容抗疲劳  多吃三种美食,润肠排毒,美容养颜,滋养子宫
多吃三种美食,润肠排毒,美容养颜,滋养子宫  天天吃二甲双胍,为何血糖不降反升?
天天吃二甲双胍,为何血糖不降反升? 