

2月10日,礼来和罗氏分别宣布,Solanezumab(索拉珠单抗)和Gantenerumab(甘特珠单抗)用于常染色体显性遗传阿尔茨海默氏病(ADAD)患者症状改善的研究中未达到主要终点。
该项研究名为DIAN-TU,是一项II/III期随机、双盲、安慰剂对照研究。测试了礼来solanezumab和罗氏gantenerumab与安慰剂相比,减缓已知患有遗传性阿尔茨海默氏病患者认知衰退率并改善疾病相关的生物标记物。该研究的主要终点指标是一种新颖的指标——DIAN多元认知终点,包括Wechsler记忆量表修订的逻辑记忆延迟召回、Cogstate国际购物清单测试、Wechsler成人智力量表修订的数字符号替代测试以及迷你精神状态检查,旨在评估ADAD患者的认知表现。
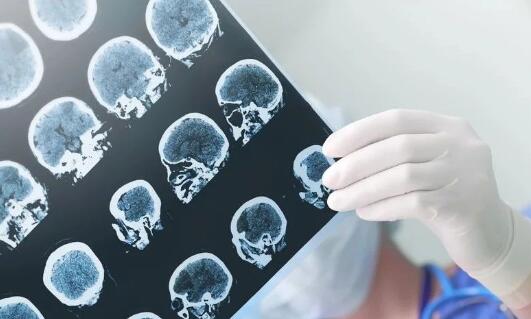
ADAD也称为家族性AD或显性遗传AD(DIAD),是一种罕见的遗传形式的AD,由APP、PSEN1或PSEN2基因中的单个基因突变引起,而由基因突变引起的AD患者占全球所有患者的比例不足1%。
DIAN-TU研究对194名参与者进行了长达7年的随访,平均时间约5年,在美国、加拿大、法国等国家设有24个研究点。在这项研究中,52人被随机分配到gantenerumab组中,50人在solanezumab组,40人在安慰剂组。所有参与者均来自携带导致遗传性的ADAD基因突变的家庭。研究包括入组时尚未出现症状的患者,以及已经有轻度症状的患者。在最短四年的治疗期中,每年跟踪一次参与者的认知度,将这些结果进行合并以得出综合评分。
罗氏表示,在这项研究中,用新型DIAN多元认知终点法测得接受gantenerumab治疗患者的认知能力下降速度没有明显减慢。总体而言,gantenerumab在DIAN-TU-001中的安全性与研究药物的其他临床试验一致,未发现新的安全性问题。使用gantenerumab最常见不良事件为注射部位反应、鼻子和喉咙感染(鼻咽炎)以及与淀粉样蛋白相关的成像异常,表现为脑水肿或微出血,大部分发现无症状。
礼来指出,36名solanezumab组患者完成了最短四年的治疗。最初的研究剂量为每四周400mg,在修正剂量后,只有25%患者的用药剂量处于较高水平。无论如何,solanezumab未达到该研究主要终点。这是礼来第四次试图证明该实验性药物能延缓神经退行性疾病患者的认知能力下降,然而与前三次结果相同,还是失败了。礼来正在进行有关次要终点和生物标志物的其他分析,结果将在今年4月的“阿尔茨海默氏症和帕金森疗法的进展焦点会议”上发表。基于主要终点的结果,礼来目前不打算让ADAD患者继续接受solanezumab治疗。
Solanezumab是一种研究型抗淀粉样蛋白单克隆抗体,结合淀粉样β肽,阻止后者在大脑中聚集并形成斑块。该药正在临床前AD患者接受抗淀粉样蛋白治疗的“无症状阿尔茨海默氏症(A4)研究”中进行试验。A4研究旨在对大脑中有淀粉样蛋白、但没有记忆力减退迹象的老年人进行solanezumab治疗的测试。
Gantenerumab是一种研究药物,旨在与β-淀粉样蛋白的聚集形式结合并去除被认为可导致脑细胞死亡的β-淀粉样蛋白斑块。此前临床研究表明,该药可使得常见形式、不是直接由基因突变引起的AD患者的β-淀粉样蛋白斑减少。罗氏目前正在进行两项III期研究(NCT01224106和NCT02051608),评估gantenerumab在前期和中期AD患者的安全性和有效性。
参考来源:
1、Lilly and Roche's antibodies fail late-phase Alzheimer's test
2、礼来、罗氏官网等。
 乳腺癌容易盯上哪些人?
乳腺癌容易盯上哪些人?  白带发黄是宫颈癌的警示吗?
白带发黄是宫颈癌的警示吗?  超高龄生育,这几件事你准备好了吗?
超高龄生育,这几件事你准备好了吗?  孩子发烧、恶心、呕吐!竟然是心理出了问题
孩子发烧、恶心、呕吐!竟然是心理出了问题  数据显示我国女性平均预期寿命突破80岁
数据显示我国女性平均预期寿命突破80岁  健康早知道:你的子宫还“年轻”吗?
健康早知道:你的子宫还“年轻”吗?  打了胰岛素,血糖为什么没有降?
打了胰岛素,血糖为什么没有降?  多囊卵巢,如何才能尽快怀孕?
多囊卵巢,如何才能尽快怀孕?  女性更年期如何保持健康与美丽?
女性更年期如何保持健康与美丽?  坚持早睡身体会有什么变化?
坚持早睡身体会有什么变化?  抑郁的人,这4类食物尽量少碰,或助改善情绪
抑郁的人,这4类食物尽量少碰,或助改善情绪  多吃3样粗粮,健脾胃,营养滋补暖身
多吃3样粗粮,健脾胃,营养滋补暖身  南京一男子每天1包烟4年2次心梗
南京一男子每天1包烟4年2次心梗  小小“杨桃”是个宝,养颜美容抗疲劳
小小“杨桃”是个宝,养颜美容抗疲劳  多吃三种美食,润肠排毒,美容养颜,滋养子宫
多吃三种美食,润肠排毒,美容养颜,滋养子宫  天天吃二甲双胍,为何血糖不降反升?
天天吃二甲双胍,为何血糖不降反升? 